Формула карбоксилна киселина в Chemistry
Карбоксилна киселина - органични съединения, чиито молекули съдържат една или повече функционални карбоксилни групи-COOH, свързан с въглеводороден радикал.
Карбоксилната група включва карбонил групи> С = О и свързаните с хидроксилна група -ОН.
Общата формула на карбоксилна киселина
Общата формула на карбоксилни киселини: R-СООН.
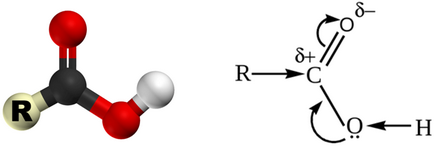
Киселинните свойства се дължат на изместване на карбоксилни киселини електронната плътност на кислород карбонил, което води до частична положителен заряд на водородния атом.
В резултат полярността на увеличенията на О-Н и става възможно процес дисоциация:
Полученият анион се стабилизира чрез зареждане делокализация:
Долна карбоксилни киселини, съдържащи до 3 въглеродни атома, - безцветна течност с характерна остра миризма, смесва се с вода във всякакви пропорции. Повечето киселини, съдържащи 4-9 въглеродни атома - маслена течност с неприятна миризма. Киселина, съдържаща повече от 10 водородни атоми - твърдите вещества, които са неразтворими във вода.
Разтворимостта на карбоксилна киселина във вода и висока точка на кипене, свързани с образуването на междумолекулни водородни връзки. В твърдо състояние съществува карбоксилна киселина най-вече под формата на цикличните димери, както се случва в течността и линеен асоциация:
Видове карбоксилни киселини
В зависимост от структурата на въглеводороден радикал, карбоксилни киселини са разделени на:
- ароматен (бензоена киселина)
- алифатен (граница (капронова киселина) и ненаситен (акрилова киселина))
- алициклен (хининова киселина)
- хетероцикличен (никотинова киселина).
Според броя на карбоксилни групи на карбоксилна киселина се разделят на:
- едноосновен (оцетна киселина)
- дикиселина (оксалова киселина)
- полиосновна (лимонена киселина).
Когато се въвежда в молекулата други киселинни функционални групи (. OH, = CO, -NH2, и т.н.) са оформени други класове от съединения: хидрокси, кето, аминокиселини и други.
Общата формула на границата на едноосновни карбоксилни киселини:
Общата формула на ненаситени монокарбоксилни киселини:
Общата формула на границата на двуосновни карбоксилни киселини:
Имената и някои карбоксилни киселини с формула
В три еднакви тръби без подписи три киселини: мравчена, оцетна и солна киселина. Както въз основа на разликите в техните химични свойства определят кои киселина присъства във всяка епруветка?
Мравчена киселина и проявява някои свойства на алдехид (намаляване). Поради това може да се определи. например, чрез взаимодействие с хидроксид на мед (II), е оформен от меден оксид в случай на мравчена киселина (I) Червено:
Може да се прави разлика между останалите киселина чрез взаимодействие със сребърен нитрат. В случай на солна киселина, бяла утайка от сребърен хлорид:
Сребърен ацетат е разтворим във вода, така че ще се случи в ин витро с промени оцетна киселина.
Така, в останалата тръба - оцетна киселина.
Определя формула естер. ако неговата хидролиза проба с тегло 2.64 грама се разпределя 1,38 грама на алкохол и 1.8 грама на моноосновен карбоксилна киселина.
Общата формула на естера състои от алкохол и киселина на различни въглеродни атоми:
По този начин, алкохол с формула:
киселина и формулата:
Уравнението на хидролиза на естер:
В съответствие със закона на масови опазване вещества, теглото на продуктите на реакцията, равна на масата на изходните материали. Ние изчисляваме масата на вода:
m (киселина) + m (алкохол) - М (естер) г
Ние изчисляваме количеството вода вещество:
Съгласно уравнението на реакцията
п (киселина) = N (алкохол) мол
Намираме моларната маса на алкохол и киселина:
Намираме коефициентите м и п от киселина и алкохол с формула:
Формула киселина СН3 СООН - оцетна киселина
Формула алкохол С2 Н5 ОН - етанол.
Така, формулата на естера СН3 COOC2 H5 - етил ацетат, етил ацетат.