Химичните свойства на карбоксилни киселини и методи за получаване на
Едноосновен карбоксилни киселини, съставени от въглероден скелет и само една карбоксилна функционална група. Всеки студент знае химични свойства на карбоксилни киселини. клас 10 обучение по програма химия включва директно изучава свойствата на едноосновни киселини. Двуосновен и многовалентни киселини имат в структурата си две или повече карбоксилни групи, съответно.
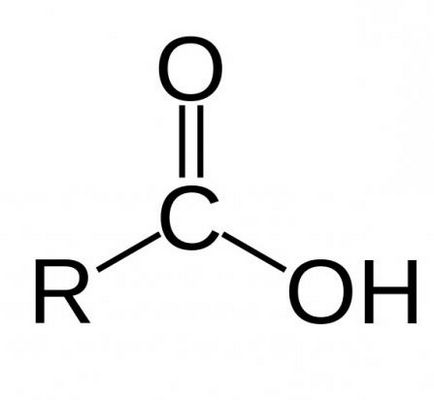
Също така, наличието или отсъствието на двойни и тройни връзки в молекулата са наситени и ненаситени карбоксилни киселини. Химични свойства и техните разлики са обсъдени по-долу.
Ако органичната киселина има състав на радикал, заместен атом, в името включени име заместваща група. Така, ако водородният атом е заместен с халоген, киселината ще присъства име заглавието халоген. Подобни промени ще претърпят наименование, ако има заместване на алдехидни, хидроксилни или амино групи.
Изомерия органични карбоксилни киселини
На практика всички органични материали имат способността да изомеризация. Карбоксилната киселина не е изключение. Следните видове изомерия:
- Въглеродният скелет.
- Interclass изомери.
- Региоизомери;
Izomerizirovatsya възможност да повлияе директно химичните свойства на карбоксилни киселини.
Изомерия скелет възможно за киселини, чийто въглеводороден радикал съдържа най-малко четири въглеродни атома. Interclass, в възможно ред за киселини с два въглеродни атома в радикал. Пространствен състояние да карбоксилни киселини с само единични връзки в скелета.
Преброяване и критична карбоксилна киселина
Карбонова киселина: химичен състав
За по-подробно разбиране на карбоксилни киселини погледнете техните свойства. В училище програма в голямо количество счита едноосновни карбоксилни киселини, химически свойства, които се проявяват в реакциите между халогеноводород, вода и други вещества. Всички такива киселина:
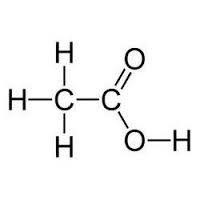
- Разпадат във разтвор на водородни йони и карбокси радикал. В този случай се отнася до мравчена киселина Електролити средна якост и слаб оцетна, т.е. силата на дисоциация намалява по хомоложна серия.
- Оцветени с лакмусова хартия червено.
- Провеждане на постоянен ток.
- Реагират с халогени: 2RCOOH + Cl2 = 2RCOOCl + 2HCl.
- Въвеждане в реакцията на естерификация с алкохол: R-COOH + R'OH = RCOOR '+ H2O.
- Взаимодействат с някои метали: RCOOH + Mg = RCOOMg + Н2.
- Реагират с основни оксиди и хидроксиди на типа образуват соли: RCOOH + NaOH = RCOONa + H2O.
- Реагира със соли: RCOOH + Na2CO3 = RCOONa + H2O + СО2.
Такива свойства са обяснени от промяната на моноосновен киселини карбоксилна група на хидроксилната група, която електроните преминаване към най-близкия въглероден атом, частично охлаждане си положителен заряд. В допълнение, карбоксилната киселина, химичните свойства на които са описани по-горе, има двупосочна взаимодействие между атоми.
Химичните свойства на други монокарбоксилни киселини
От класификацията известно, че има едноосновен ненаситена карбоксилна киселина, химичните свойства на които се различават от тези на ограничението.
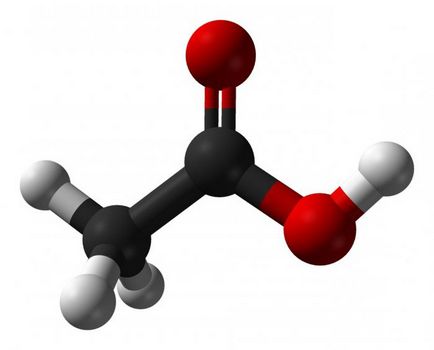
По този начин, киселината с двойна връзка в въглеводороден радикал - моноосновен ненаситени карбоксилни киселини. химичните свойства на такива киселини са дадени в реакции:
- Тъй като халогеноводород, но много по-бавно граници и в противоречие с правило Markovnikov, както карбоксилната група намалява електронната плътност на двойна връзка: R = СН-СООН + HCl = RCL-СН2-СООН.
- С халогена: Br2 + R = СН-СООН = RBr-CHBr-СООН.
- Тъй като водород, в резултат на прекъсвания на двойната връзка: H2 + R = СН-СООН = СООН-R-СН.
- Внимателно окисление, което води до образуване на оксикиселини: R = СН-СООН + H2O [O] R (ОН) -СН (ОН) СООН.
- Радикална окисляване срещащи с разкъсване киселинни молекули (например акрилова киселина): СН3-СН = С-СООН + H2O [O] CH3COOH + НООС-СООН.
- Полимеризацията: п СООН- (СН = СН) -R = N (-СООН-СН-СН-R-)
Химични свойства dvukarbonovyh киселини
Дикарбоксилна органични киселини - дикарбоксилна киселина. Химичните свойства на такива монокарбоксилни киселини се различават от свойства. Това се дължи на факта, че силата на двуосновни киселини едноосновен повече енергия, поради влиянието на втората група на карбоксил и хидроксил. Докато този ефект намалява с разстоянието от верига от въглеродни атоми.
Двуосновен киселини имат следните свойства:
- Декарбоксилирането на киселини (например etandinovoy): НООС-COOH (т) = НООС + СО2. Важно е да се знае, че оксаловата киселина и малонова киселина се подлага на декарбоксилиране е много по-лесно, отколкото други.
- Образуването на киселина соли и вторичен: HOOC-R-R-COOK или HOOK-R-R-COOK.
- Образуването на пълни и частични естери.
- Малонова киселина е способна да претърпи реакция на заместване на водород от групата СН2-въглеводород радикал лесно заменен с метални атоми.
Соли с карбоксилни киселини
Соли - са органични съединения, образувани чрез заместване на водородния атом на хидроксилни и карбоксилни групи на карбоксилна киселина към метала. Това е, органични киселини в реакции с неорганични основи или соли са способни да образуват соли на карбоксилни киселини. Химични свойства, които са получени от такива органични съединения, като соли, се използват в промишлеността за производство на домакински сапун.
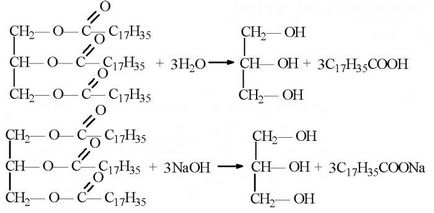
Особено подходящи за синтез на твърди и течни сапуни са стеаринова (октадеканова) и палмитинова (хексадеканова киселина). Също така често се използва олеинова (цис-9-октадеценова) и миристинова (тетрадеканова киселина) киселина.
основа Реакцията на получаване на сапуни е над синтеза на естери на киселини с калиев или натриев сол.
Методи за получаване на карбоксилни киселини
Начини и методи за получаване на киселини с СООН група, има много, но най-често използваните са:
- Изолиране от природни вещества (мазнини и т.н.).
- Окисляване с моноалкохоли или СОН-група на съединения (алдехиди): ROH (RCOH) [O] R-COOH.
- Хидролиза с алкален trigalogenalkanov получава междинно съединение моноалкохол: RCl3 + NaOH = (ROH + 3NaCl) = RCOOH + H2O.
- Осапунването или хидролиза на естер и алкохол (естери): R-COOR '+ NaOH = (R-COONa + R'OH) = R-COOH + NaCl.
- Перманганат окисление на алкани (твърд окисляване): R = СН2 [O], (KMnO4) RCOOH.
Значение на карбоксилни киселини за човека и промишленост

Химичните свойства на карбоксилни киселини са важни за човешкия живот. Те са много важни за организма, тъй като в големи количества, съдържащи се във всяка клетка. Метаболизмът на мазнини, протеини и въглехидрати винаги преминава през етапа, на който единият или другият се получава карбоксилна киселина.
В допълнение, карбоксилна киселина, използвана в създаването на лекарства. Никой от фармацевтичната индустрия не може да съществува без всъщност свойства на органични киселини.

Важната роля на съединението с карбоксилна група и играта в козметичната индустрия. Синтез на мазнини за последващо производство на сапуни, детергенти и битовата химия въз основа на реакцията на естерификация с карбоксилна киселина.
Химичните свойства на карбоксилни киселини са отразени в живота на човек. Те имат, както и в големи количества, съдържащи се във всяка клетка от голямо значение за човешкото тяло. Метаболизмът на мазнини, протеини и въглехидрати винаги преминава през етапа, на който единият или другият се получава карбоксилна киселина.