Как да се изчисли процента на теглото
Масов процент определя процентът на елементи в химично съединение. [1] За да се определи процента на теглото е необходимо да се знае молекулна маса (грама на мол), включени в съединителните елементи или броя на грам на всеки компонент, необходимо да се получи даден разтвор. [2] Тегловният процент изчислява съвсем проста: достатъчно е да се разделят на маса елемент (или компонент) от теглото на всички на съединението (или разтвор).
стъпки Редактиране
Метод 1 от 2:
Определяне на теглото на сто от дадена маса Редактиране


- В началото на решаване на проблема, записва тегло равенство процент = (теглото на компонент / общо тегло на съединението) х 100.
- Масата на компонент на интерес трябва да бъде в проблема. Ако масата не е дадено, преминете към следващата глава, в което той говори за това, как да се определи процента от теглото на неизвестен маса.
- Общата маса на химичното съединение се получава чрез добавяне на масите на всички елементи (компоненти), които са част от това съединение (или разтвор).


- Пример 1: Какво е тегловният процент на 5 г натриев хидроксид, разтворен в 100 г вода?
- Общото тегло на разтвора е сумата от количествата на натриев хидроксид и вода: 100 гр + 5 грама дават 105 гр
- Пример 2: Колко натриев хлорид и вода, необходимо за получаване на 175 грама на 15 процент разтвор на?
- В този пример, даден от общата маса и необходимия процент, а вие искате да намерите броя на веществата, които се добавят към разтвора. Общото тегло е 175 грама.


- Пример 1: предварително определена маса на компонентите - натриев хидроксид - е 5 грама.
- Пример 2: В този пример дадено тегло на компонента е неизвестен, и трябва да бъде намерен.
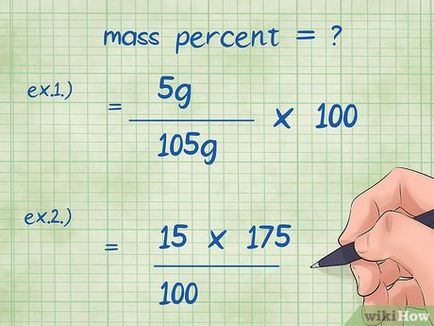
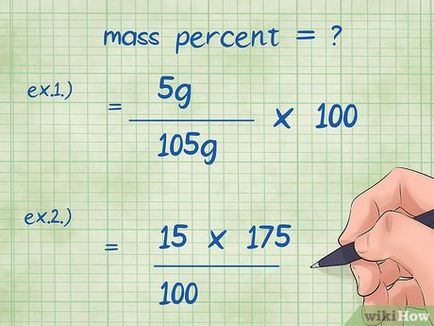
- Пример 1: тегловни процента = (тегло компонент / общата маса на съединението) х 100 = (5 г / 105 гр) х 100.
- Пример 2 трябва да се превърне в процента формула тегло, така че да бъде в състояние да открие неизвестен масата на химически компонента: компонент = маса (маса процента от общата маса на съединението *) / 100 = (15 * 175) / 100.


- Пример 1: (5/105) х 100 = 0,04761 х 100 = 4.761%. По този начин тегловният процент на 5 г натриев хидроксид, разтворен в 100 г вода е 4.761%.
- Пример 2: Експресия се пренаписва за маса процента компонент (процент от теглото на общата маса на веществото *) / 100, където намираме: (15 * 175) / 100 = (2625) / 100 = 26.25 грама натриев хлорид.
- Необходимото количество вода се получава чрез изваждане на теглото на компонент от общото тегло на разтвора: 175 - 26,25 = /148.75 грама вода.
Метод 2 на 2:
Определяне на масата на сто, когато масите не са настроени Редактиране


- В началото на решаване на проблема, записва тегловният процент равенство = (моларна маса на елемента / общо молекулно тегло на съединението) х 100.
- И двете стойности се измерват в грама на мол (г / мол).
- Ако не са дадени на тегло, процентът на теглото на компонент в даден въпрос може да се намери с помощта на моларната маса.
- Пример 1: Виж тегловният процент на водород в молекулата на водата.
- Пример 2: Виж масовия процент на въглерод в молекулата на глюкоза.


- Пример 1: запис химична формула на вода, Н2 О.
- Пример 2: Глюкоза запис химична формула, С6 Н12 О6.


- Пример 1: Виж кислород моларна маса (15,9994) и водород (1.0079). [9]
- Пример 2: Виж моларната маса на въглерод (12.0107), кислород (15,9994) и водород (1.0079).


- Пример 1: символ на водород е 2, и по кислород символ 1 (еквивалентно на липса на). По този начин, моларната маса на водород се умножава по 2: 1,00794 X 2 = 2,01588; молекулна маса на кислород остава същата, 15,9994 (т.е., умножена по 1).
- Пример 2: символ означава 6 въглеродни под водород 12 и кислород под 6. Увеличаването молна маса елементи на тези данни, ние откриваме, че:
- въглерод: (12,0107 * 6) = 72,0642
- водород: (1,00794 * 12) = 12,09528
- кислород: (15,9994 * 6) = 95,9964


- Пример 1: добави към 2.01588 грама / мол (маса на два мола водородни атоми) 15.9994 грама / мол (тегло на един мол от кислородни атоми), като резултат на това ще 18.01528грам / мол.
- Пример 2 кратен моларен маси резултати: въглерод + водород + кислород = 72,0642 + 12,09528 + 95,9964 = 180,156 г / мол.


- Пример 1: Масата на водород в съединение е 2.01588 грама / мол (маса на два мола водородни атоми).
- Пример 2: маса на въглерод в съединението е 72,0642 грама / мол (мола масови шест въглеродни атоми).


- Пример 1: тегловни процента = (моларна маса елемент / общо молекулно тегло съединение) х 100 = (2,01588 / 18,01528) х 100.
- Пример 2: тегловни процента = (моларна маса елемент / общо молекулно тегло съединение) х 100 = (72,0642 / 180.156) х 100.
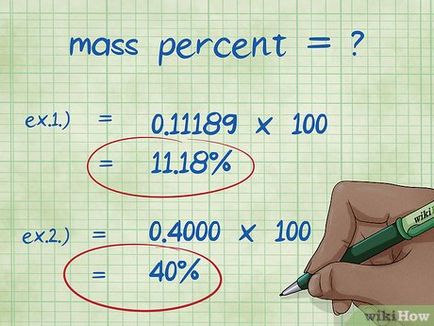
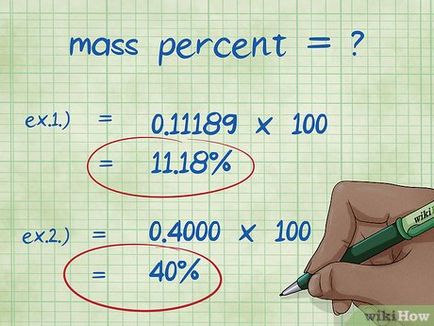
- Пример 1: тегловни процента = (моларна маса елемент / общо молекулно тегло на съединението) х 100 = (2,01588 / 18,01528) х 100 = 0,11189 х 100 = 11.18%. По този начин тегловният процент на водородните атоми в молекулата на водата е равно на 11,18%.
- Пример 2: тегловни процента = (моларна маса елемент / общо молекулно тегло на съединението) х 100 = (72,0642 / 180.156) х 100 = 0,4000 х 100 = 40.00%. По този начин тегловният процент на въглеродните атоми в молекулата на глюкоза е 40,00%.